Methyl-acetát
Methyl-acetát je organická sloučenina patřící mezi estery kyseliny octové, se vzorcem CH3COOCH3 (zkráceně AcOMe či MeOAc). Používá se ojediněle jako rozpouštědlo, lipofilní a slabě polární, častěji je ale používán podobný ethyl-acetát, který je méně toxický a méně se rozpouští ve vodě; methyl-acetát může za pokojové teploty vytvořit až 25% vodný roztok a za vyšších teplot se rozpouští ještě lépe. Ve vodných roztocích silných zásad a kyselin se rozkládá.
| Methyl-acetát | |
|---|---|
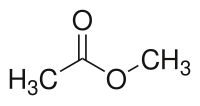 Strukturní vzorec | |
 Model molekuly | |
| Obecné | |
| Systematický název | methyl-acetát |
| Funkční vzorec | CH3COOCH3 |
| Sumární vzorec | C3H6O2 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 79-20-9 |
| EC-no (EINECS/ELINCS/NLP) | 201-185-2 |
| PubChem | 6584 |
| ChEBI | 77700 |
| SMILES | O=C(OC)C |
| InChI | 1S/C3H6O2/c1-3(4)5-2/h1-2H3 |
| Vlastnosti | |
| Molární hmotnost | 74,079 g/mol |
| Teplota tání | −98,2 °C (175,0 K)[1] |
| Teplota varu | 56,7 °C (329,8 K)[1] |
| Hustota | 0,9342 g/cm3 (20 °C)[1] |
| Rozpustnost ve vodě | 24,3 g/100 ml (20 °C)[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v ethanolu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v diethyletheru[1] |
| Tlak páry | 23,1 kPa (20 °C) 28,8 kPa (20 °C)[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H225 H319 H336[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P261 P264+265 P271 P280 P303+361+353 P304+340 P305+351+338 P319 P337+317 P370+378 P403+233 P403+235 P405 P501[1] |
| Teplota vzplanutí | −10 °C (263 K)[1] |
Některá data mohou pocházet z datové položky. | |
Výroba editovat
Methyl-acetát se získává jako vedlejší produkt karbonylace methanolu při výrobě kyseliny octové.[2] Vytvořit se může také esterifikací kyseliny octové methanolem za přítomnosti silných kyselin, například sírové; účinnost tohoto postupu lze zlepšit pomocí reaktivní destilace.
Reakce editovat
Za přítomnosti silných zásad, například hydroxidu sodného, nebo silných kyselin, jako je kyselina chlorovodíková nebo sírová, se methylacetát hydrolyzuje na methanol a kyselinu octovou; tento rozklad se urychluje s rostoucí teplotou. Reakce s kyselinou je vzhledem k esteru prvního řádu a reakce se zásadou je vůči oběma reaktantům druhého řádu.
Methylacetát funguje jako Lewisova zásada, která vytváří 1:1 adukty s Lewisovými kyselinami. Patří mezi tvrdé zásady.
Použití editovat
Methylacetát se používá jako těkavé rozpouštědlo v lepidlech, barvách a odlakovačích na nehty.
Acetanhydrid se vyrábí karbonylací methylacetátu.[3]
Odkazy editovat
Reference editovat
V tomto článku byl použit překlad textu z článku Methyl acetate na anglické Wikipedii.
- ↑ a b c d e f g h i j k l https://pubchem.ncbi.nlm.nih.gov/compound/6584
- ↑ Hosea Cheung, Robin S. Tanke, G. Paul Torrence Acetic Acid, Ullmann's Encyclopedia of Industrial Chemistry, 2002, Wiley-VCH, Weinheim DOI:10.1002/14356007.a01_045
- ↑ J. R. Zoeller; V. H. Agreda; S. L. Cook; N. L. Lafferty; S. W. Polichnowski; D. M. Pond. Eastman Chemical Company Acetic Anhydride Process. Catalysis Today. 1992, s. 73–91. DOI 10.1016/0920-5861(92)80188-S.
Související články editovat
Externí odkazy editovat
- Obrázky, zvuky či videa k tématu Methyl-acetát na Wikimedia Commons

