Dimethoxymethan
Dimethoxymethan je organická sloučenina patřící mezi ethery (jde o dimethylacetal formaldehydu), bezbarvá kapalina s nízkou viskozitou, používaná jako rozpouštědlo. Je rozpustný ve vodě a mísitelný s většinou běžných organických rozpouštědel.
| Dimethoxymethan | |
|---|---|
 Strukturní vzorec | |
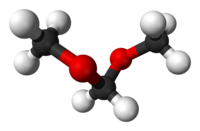 Model molekuly | |
| Obecné | |
| Systematický název | dimethoxymethan |
| Funkční vzorec | CH3OCH2OCH3 |
| Sumární vzorec | C3H8O2 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 109-87-5 |
| EC-no (EINECS/ELINCS/NLP) | 203-714-2 |
| PubChem | 8020 |
| ChEBI | 48341 |
| SMILES | COCOC |
| InChI | InChI=1S/C3H8O2/c1-4-3-5-2/h3H2,1-2H3 |
| Číslo RTECS | PA8750000 |
| Vlastnosti | |
| Molární hmotnost | 76,094 g/mol |
| Teplota tání | −105 °C (168 K)[1] |
| Teplota varu | 42 °C (315 K)[1] |
| Hustota | 0,86 g/cm3[1] |
| Rozpustnost ve vodě | 33 g/100 ml[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v acetonu a ethanolu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v benzenu a diethyletheru[1] |
| Tlak páry | 42,6 kPa (20 °C)[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H225 H315 H319 H335[1] |
| P-věty | P210 P233 P240 P241 P242 P243 P261 P264 P264+265 P271 P280 P302+352 P303+361+353 P304+340 P305+351+338 P319 P321 P332+317 P337+317 P362+364 P370+378 P403+233 P403+235 P405 P501[1] |
| Teplota vzplanutí | −32 °C (241 K)[1] |
Některá data mohou pocházet z datové položky. | |
Výroba a struktura
editovatTato látka se může vyrobit oxidací methanolu nebo reakcí formaldehydu s methanolem. Ve vodných roztocích kyselin se zpětně hydrolyzuje na formaldehyd a methanol.
Vzhledem k anomernímu efektu u dimethoxymethanu převládá židličková konformace namísto anti konformace vůči vazbám C-O. Vzhledem k tomu, že se v molekule nachází dvě vazby C–O, tak je nejstabilnější konformací židlička-židlička, s energií přibližně o 30 kJ/mol nižší než anti-anti, kde židlička-anti a anti-židlička tvoří průměr těchto energií.[2]
Protože se jedná o jednu z nejmenších molekul, u kterých se tento jev vyskytuje, tak se dimethoxymethan často používá v teoretických studiích zaměřeních na anomerní efekt a má tak význam v chemii sacharidů.
Použití
editovatPrůmyslově se dimethoxymethan využívá jako rozpouštědlo a jako výchozí látka při výrobě vůní, pryskyřic, lepidel a ochranných nátěrů. Dalším použitím je přidávání této látky do benzinu, kde zvyšuje oktanové číslo; dimethoxymethan se také přidává do motorových naft.[3]
V organické syntéze
editovatDimethoxymethan může také sloužit v organické syntéze k tvorbě methoxymethylových (MOM) chránicích skupin pro alkoholy.[4] Tyto skupiny se oobvykle vytvářejí reakcemi s oxidem fosforečným v dichlormethanu nebo chloroformu, což je postup upřednostňovaný před použitím chlormethylmethyletheru (MOMCl), který lze připravit jako roztok v methylesteru reakcí dimethoxymethanu a acylchloridu za přítomnosti katalyzátoru v podobě Lewisovy kyseliny, jako je například bromid zinečnatý:
- MeOCH2OMe + RC(=O)Cl → MeOCH2Cl + RC(=O)(OMe)
Roztok reaktantu je možné použít přímo bez přečišťování, což omezuje styk s karcinogenním chlormethylmethyletherem. Na rozdíl od postupu využívajícího formaldehyd a chlorovodík zde nevzniká vysoce karcinogenní vedlejší produkt bis(chlormethyl)ether.[5]
Odkazy
editovatExterní odkazy
editovat- Obrázky, zvuky či videa k tématu Dimethoxymethan na Wikimedia Commons
Reference
editovatV tomto článku byl použit překlad textu z článku Dimethoxymethane na anglické Wikipedii.
- ↑ a b c d e f g h i j k l https://pubchem.ncbi.nlm.nih.gov/compound/8020
- ↑ Francis A. Carey; Richard J. Sundberg. Advanced organic chemistry. New York: Springer, 2007. ISBN 9780387448978.
- ↑ Krishna P. Shrestha, Sven Eckart, Ayman M. Elbaz, Binod R. Giri, Chris Fritsche, Lars Seidel, William L. Roberts, Hartmut Krause, Fabian Mauss. A comprehensive kinetic model for dimethyl ether and dimethoxymethane oxidation and NO interaction utilizing experimental laminar flame speed measurements at elevated pressure and temperature. Combustion and Flame. 2020, s. 57–74. DOI 10.1016/j.combustflame.2020.04.016.
- ↑ MARTIN BERLINER, KATHERINE BELECKI. Synthesis of Alpha-Halo Ethers from Symmetric Acetals and in situ Methoxymethylation of an Alcohol. Org. Synth.. S. 102. Dostupné online.; Coll. Vol.. S. 934.
- ↑ SYNTHESIS OF ALPHA-HALO ETHERS FROM SYMMETRIC ACETALS AND in situ METHOXYMETHYLATION OF AN ALCOHOL [online]. [cit. 2018-09-13]. Dostupné online.

