Střevní mikroflóra
Střevní mikroflóra (mikrobiom) jsou mikroorganismy, které žijí v trávicí soustavě živočichů včetně člověka. Mnohdy hostiteli prospívají, někdy však mohou i škodit.


V lidských střevech je přibližně 1013–1014 bakterií, přičemž buněk lidského těla je asi 1013. Jinými slovy, bakterií v lidském těle je stejně či až desetkrát více, než lidských buněk samotných.[1][2] Celkem ve střevě žije asi 500 druhů bakterií.[3] Hmotnostné dominantními mikroorganismy v tlustém střevě jsou bakterie, ty ve výsledku tvoří 60 % hmotnosti stolice.[4] Devadesát devět procent těchto bakterií však pochází z 30–40 nejběžnějších druhů.[5] Mimo bakterie jsou častými mikroorganismy v střevech i různé houby,[6] prvoci a viry (identifikováno přes 50 tisíc druhů virů),[7] o nichž se však zatím ví jen málo. Mikroflóra je specifická pro daného člověka.[8] Mikroflóra souvisí se stravou[9] i cvičením.[10] Silný vliv na složení střevní mikroflóry mají léky, které užíváme, např. se mění v reakci na imunoterapii nebo na chemoterapii.[11] Vliv má i sexuální chování a s ním spojené praktiky.[12]
Symbiotický vztah
editovatVědci se domnívají, že vztah mezi člověkem a mikroorganismy není komenzálismus (jednostranně výhodný vztah), ale spíše mutualismus (oboustranně výhodný vztah). Přestože lidé mohou žít bez střevní flóry, mikroorganismy vykonávají řadu užitečných funkcí. Fermentují nestrávené organické látky z potravy jako například celulózu na cukry, které pak mohou být využity jako zdroj energie.[13][14] Formují imunitní systém skrze uvolňování různých strukturních molekul a metabolických produktů, které následně regulují imunitní buňky.[15][16][17] Mnoho z imunomodulačních molekul zdravé mikroflóry je spjato s protizánětlivými nebo imunosupresivnímy účinky jako například Polysacharid A či mastné kyseliny s krátkým řetězcem.[18][16] Střevní mikroflóra dále zamezuje růstu patogenních druhů mikroorganismů a to buď jednoduše svou přítomností (tedy obsazením niky) nebo aktivní produkcí antimikrobiálních látek.[19] Mikrobiom ovlivňuje i vývoj střeva dodáváním zdrojů energie pro růst a stimulací bariérové funkce.[20][21] Efekt střevní mikroflóry však sahá i mimo střevo a to nejen systémovým rozšířením imunitních buněk ale i produkcí (popřípadě stimulací produkce) hormonů a neurotransmiterů.[22][23]
Symbiotický vztah může být narušen dysbiózou tedy stavem, kdy je složení mikrobiomu mimo rovnováhu. Některé druhy bakterií, které jsou ve zdravém složení neškodné se mohou stát v jiném kontextu oportunními patogeny.[24] Jiné mikroby jsou obligátně patogenní a mutualistický vztah s hostitelem neustavují vůbec. Dysbióza střevní mikroflóry může vést k narušení stimulů poskytovaných mikroby a je také proto spojována s onemocněními jako alergie, nespecifický střevní zánět nebo kolorektální karcinom.[25][26][27]
Mikroflóra u kojenců
editovatBezprostředně před porodem je střevo plodu sterilní. Během porodu se do novorozence dostávají mikroby (Escherichia coli a enterokoky) z porodních cest matky, což ale neplatí pro porod císařským řezem. Skrze mateřské mléko kojenec čerpá především laktobacily a bifidobakterie z mléčných žláz, mimo toho mateřské mléko obsahuje ochranné faktory a mléčný cukr laktózu. Pokud se všechna laktóza nestačí v tenkém střevě rozložit, stane se v tlustém střevě potravou pro bifidobakterie, které u kojenců tvoří 90% střevní mikroflóry. Rozkladem laktózy vzniká kyselina mléčná, která zabraňuje usídlení patogenních bakterií. S přechodem na tuhou stravu četnost bifidobakterií klesá. Také antibiotika omezují mikroflóru. Složení také může mít vliv na rozvoj mozku.[28] Část mikroflóry se získává od otců a jiných zdrojů.[29]
Druhy mikroorganismů
editovatVětšina bakterií mikroflóry patří do rodů Bacteroides, Clostridium, Fusobacterium,[5] dále Eubacterium, Ruminococcus, Peptococcus, Peptostreptococcus a Bifidobacterium.[5] Výrazně nejčastější je rod Bacteroides, který tvoří 30 % všech bakterií v střevě. Další rody, jako Escherichia a Lactobacillus, tak časté nejsou.
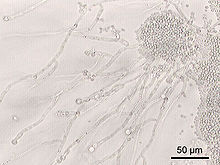
Z hub se ve střevech vyskytují rody Candida (Candida albicans), Saccharomyces (např. známá pivní kvasinka), Aspergillus a Penicillium (štětičkovec). V střevě se vyskytují též archebakterie, jako zejména druh Methanobrevibacter smithii.[30]
Metabolismus bakterií
editovatVe střevě existují bakterie hnilobné, které produkují amoniak, sulfan a různé fenoly, a bakterie kvasné, které produkují methan a oxid uhličitý.
Související články
editovatReference
editovatV tomto článku byl použit překlad textu z článku Gut flora na anglické Wikipedii.
- ↑ GUARNER, Francisco; MALAGELADA, Juan-R. Gut flora in health and disease. S. 512–519. The Lancet [online]. 2003-02 [cit. 2020-11-25]. Roč. 361, čís. 9356, s. 512–519. DOI 10.1016/S0140-6736(03)12489-0. PMID 12583961. (anglicky)
- ↑ SENDER, Ron; FUCHS, Shai; MILO, Ron. Are We Really Vastly Outnumbered? Revisiting the Ratio of Bacterial to Host Cells in Humans. Cell. 2016-01-28, roč. 164, čís. 3, s. 337–340. Dostupné online [cit. 2016-02-12]. ISSN 1097-4172. DOI 10.1016/j.cell.2016.01.013. PMID 26824647. (anglicky)
- ↑ GIBSON, Glenn R. Fibre and effects on probiotics (the prebiotic concept). S. 25–31. Clinical Nutrition Supplements [online]. 2004-01-01 [cit. 2020-11-25]. Roč. 1, čís. 2, s. 25–31. DOI 10.1016/j.clnu.2004.09.005. (anglicky)
- ↑ STEPHEN, A. M.; CUMMINGS, J. H. The Microbial Contribution to Human Faecal Mass. Journal of Medical Microbiology. 1980, s. 45–56. DOI 10.1099/00222615-13-1-45. PMID 7359576.
- ↑ a b c BEAUGERIE, Laurent; PETIT, Jean-Claude. Microbial-gut interactions in health and disease. Antibiotic-associated diarrhoea. S. 337–352. Best Practice & Research Clinical Gastroenterology [online]. 2004-04 [cit. 2020-11-25]. Roč. 18, čís. 2, s. 337–352. DOI 10.1016/j.bpg.2003.10.002. PMID 15123074. (anglicky)
- ↑ Fungi in the gut prime immunity against infection. phys.org [online]. 2021-02-06 [cit. 2022-01-09]. Dostupné online. (anglicky)
- ↑ HUGENHOLTZ, Philip; LOW, Soo Jen. Study: 92% of viruses in gut microbiome were previously unknown to science. sciencex.com [online]. 2021-06-25 [cit. 2022-01-09]. Dostupné online. (anglicky)
- ↑ Our bacteria are more personal than we thought, new study shows. phys.org [online]. [cit. 2024-03-13]. Dostupné online.
- ↑ Hunter-gatherers' seasonal gut-microbe diversity loss echoes our permanent one. phys.org [online]. 2017-08-24 [cit. 2020-11-25]. Dostupné online. (anglicky)
- ↑ YATES, Diana. Exercise changes gut microbial composition independent of diet, team reports. medicalxpress.com [online]. 2017-12-04 [cit. 2020-11-25]. Dostupné online. (anglicky)
- ↑ ŠUTA, Miroslav; ŠŤOVÍČEK, Vladimír. Škůdce, nebo pomocník? Střevní bakterie svedou obojí. Český rozhlas Plzeň [online]. 2019-03-03 [cit. 2020-11-25]. Dostupné online.
- ↑ Biodiversity of gut bacteria is associated with sexual behavior. medicalxpress.com [online]. [cit. 2024-02-27]. Dostupné online.
- ↑ ROBERT, Céline; BERNALIER-DONADILLE, Annick. The cellulolytic microflora of the human colon: evidence of microcrystalline cellulose-degrading bacteria in methane-excreting subjects. FEMS microbiology ecology. 2003-10-01, roč. 46, čís. 1, s. 81–89. PMID: 19719585. Dostupné online [cit. 2019-02-13]. ISSN 1574-6941. DOI 10.1016/S0168-6496(03)00207-1. PMID 19719585.
- ↑ ROEDIGER, W. E. Utilization of nutrients by isolated epithelial cells of the rat colon. Gastroenterology. 1982-8, roč. 83, čís. 2, s. 424–429. PMID: 7084619. Dostupné online [cit. 2019-02-13]. ISSN 0016-5085. PMID 7084619.
- ↑ MASLOWSKI, Kendle M.; VIEIRA, Angelica T.; NG, Aylwin. Regulation of inflammatory responses by gut microbiota and chemoattractant receptor GPR43. Nature. 2009-10-29, roč. 461, čís. 7268, s. 1282–1286. PMID: 19865172 PMCID: PMC3256734. Dostupné online [cit. 2019-02-13]. ISSN 1476-4687. DOI 10.1038/nature08530. PMID 19865172.
- ↑ a b VINOLO, Marco A. R.; RODRIGUES, Hosana G.; HATANAKA, Elaine. Suppressive effect of short-chain fatty acids on production of proinflammatory mediators by neutrophils. The Journal of Nutritional Biochemistry. 2011-9, roč. 22, čís. 9, s. 849–855. Dostupné online [cit. 2019-02-13]. ISSN 1873-4847. DOI 10.1016/j.jnutbio.2010.07.009. PMID 21167700. (anglicky)
- ↑ JOHNSON, Jenny L.; JONES, Mark B.; COBB, Brian A. Polysaccharide A from the capsule of Bacteroides fragilis induces clonal CD4+ T cell expansion. The Journal of Biological Chemistry. 2015-02-20, roč. 290, čís. 8, s. 5007–5014. Dostupné online [cit. 2019-02-13]. ISSN 1083-351X. DOI 10.1074/jbc.M114.621771. PMID 25540199. (anglicky PMCID: PMC4335237)
- ↑ DASGUPTA, Suryasarathi; ERTURK-HASDEMIR, Deniz; OCHOA-REPARAZ, Javier. Plasmacytoid dendritic cells mediate anti-inflammatory responses to a gut commensal molecule via both innate and adaptive mechanisms. Cell Host & Microbe. 2014-04-09, roč. 15, čís. 4, s. 413–423. Dostupné online [cit. 2019-02-13]. ISSN 1934-6069. DOI 10.1016/j.chom.2014.03.006. PMID 24721570. (anglicky PMCID: PMC4020153)
- ↑ TASAKIS, Rafail Nikolaos; TOURAKI, Maria. Identification of bacteriocins secreted by the probiotic Lactococcus lactis following microwave-assisted acid hydrolysis (MAAH), amino acid content analysis, and bioinformatics. Analytical and Bioanalytical Chemistry. 2018-2, roč. 410, čís. 4, s. 1299–1310. Dostupné online [cit. 2019-02-13]. ISSN 1618-2650. DOI 10.1007/s00216-017-0770-3. PMID 29256074. (anglicky)
- ↑ PENG, Luying; LI, Zhong-Rong; GREEN, Robert S. Butyrate enhances the intestinal barrier by facilitating tight junction assembly via activation of AMP-activated protein kinase in Caco-2 cell monolayers. The Journal of Nutrition. 2009-9, roč. 139, čís. 9, s. 1619–1625. PMC2728689. Dostupné online [cit. 2019-02-13]. ISSN 1541-6100. DOI 10.3945/jn.109.104638. PMID 19625695. (anglicky)
- ↑ MACK, D. R.; MICHAIL, S.; WEI, S. Probiotics inhibit enteropathogenic E. coli adherence in vitro by inducing intestinal mucin gene expression. The American Journal of Physiology. 04 1999, roč. 276, čís. 4, s. G941–950. Dostupné online [cit. 2019-02-13]. ISSN 0002-9513. DOI 10.1152/ajpgi.1999.276.4.G941. PMID 10198338. (anglicky)
- ↑ YANO, Jessica M.; YU, Kristie; DONALDSON, Gregory P. Indigenous bacteria from the gut microbiota regulate host serotonin biosynthesis. Cell. 2015-04-09, roč. 161, čís. 2, s. 264–276. PMCID: PMC4393509. Dostupné online [cit. 2019-02-13]. ISSN 1097-4172. DOI 10.1016/j.cell.2015.02.047. PMID 25860609. (anglicky)
- ↑ ASANO, Yasunari; HIRAMOTO, Tetsuya; NISHINO, Ryo. Critical role of gut microbiota in the production of biologically active, free catecholamines in the gut lumen of mice. American Journal of Physiology. Gastrointestinal and Liver Physiology. 2012-12-01, roč. 303, čís. 11, s. G1288–1295. Dostupné online [cit. 2019-02-13]. ISSN 1522-1547. DOI 10.1152/ajpgi.00341.2012. PMID 23064760. (anglicky)
- ↑ THAKKAR, Shyam; AGRAWAL, Radheshyam. A Case of Staphylococcus aureus Enterocolitis: A Rare Entity. Gastroenterology & Hepatology. 2010-2, roč. 6, čís. 2, s. 115–117. PMCID: PMC2886449. Dostupné online [cit. 2019-02-13]. ISSN 1554-7914. PMID 20567553. (anglicky)
- ↑ JOHANSSON, Maria A.; SJÖGREN, Ylva M.; PERSSON, Jan-Olov. Early colonization with a group of Lactobacilli decreases the risk for allergy at five years of age despite allergic heredity. PloS One. 2011, roč. 6, čís. 8, s. e23031. PMCID: PMC3148229. Dostupné online [cit. 2019-02-13]. ISSN 1932-6203. DOI 10.1371/journal.pone.0023031. PMID 21829685. (anglicky)
- ↑ WALDECKER, Markus; KAUTENBURGER, Tanja; DAUMANN, Heike. Inhibition of histone-deacetylase activity by short-chain fatty acids and some polyphenol metabolites formed in the colon. The Journal of Nutritional Biochemistry. 2008-9, roč. 19, čís. 9, s. 587–593. PMID: 18061431. Dostupné online [cit. 2019-02-13]. ISSN 0955-2863. DOI 10.1016/j.jnutbio.2007.08.002. PMID 18061431. (anglicky)
- ↑ MAZMANIAN, Sarkis K.; ROUND, June L.; KASPER, Dennis L. A microbial symbiosis factor prevents intestinal inflammatory disease. Nature. 2008-05-29, roč. 453, čís. 7195, s. 620–625. PMID: 18509436. Dostupné online [cit. 2019-02-13]. ISSN 1476-4687. DOI 10.1038/nature07008. PMID 18509436. (anglicky)
- ↑ Research hints at links between babies' microbiome and brain development. medicalxpress.com [online]. [cit. 2023-08-09]. Dostupné online.
- ↑ Study shows role of fathers in seeding microbiota of newborns, confirms benefits of maternal fecal microbiota transfer. medicalxpress.com [online]. [cit. 2024-06-12]. Dostupné online.
- ↑ DERMOUMI, Heide L.; ANSORG, Rainer A.M. Isolation and Antimicrobial Susceptibility Testing of Fecal Strains of the Archaeon Methanobrevibacter smithii. S. 177–183. Chemotherapy [online]. 2001 [cit. 2020-11-25]. Roč. 47, čís. 3, s. 177–183. DOI 10.1159/000063219. (anglicky)
Externí odkazy
editovat- Obrázky, zvuky či videa k tématu střevní mikroflóra na Wikimedia Commons