Dendrimer
Dendrimery (také se používají označení arboroly, dendrony a kaskádové molekuly) jsou vysoce uspořádané polymery s rozvětvenými molekulami.[1][2]

Molekuly dendrimerů jsou obvykle souměrné podle svých středů a často zaujímají kulovitý tvar. Většinou obsahují chemicky dostupnou funkční skupinu, nazývanou ohnisko nebo jádro. Rozdíly mezi dendrimery a dendrony jsou zobrazeny výše; tyto pojmy se však často zaměňují.[3]
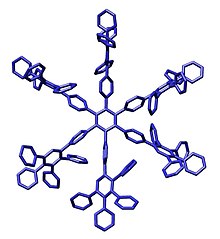
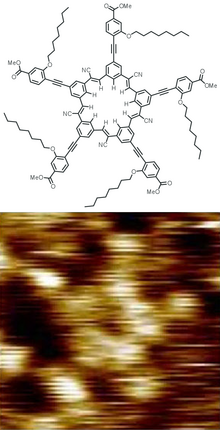
První dendrimery připravili Fritz Vögtle v roce 1978 divergentní syntézou,[6] R. G. Denkewalter v roce 1981,[7][8] Donald Tomalia roku 1983[9] a 1985[10][11] a ve stejném roce i George R. Newkome.[12]
V roce 1990 vyvinuli Craig Hawker a Jean Fréchet konvergentní metodu přípravy.[13]
Příprava
editovatJeden z prvních dendrimerů, Newkomeův dendrimer, byl připraven v roce 1985. Na obrázku výše je zobrazen mechanismus přípravy prvních dvou generací divergentním způsobem. Nejprve se provede nukleofilní substituce 1-bromopentanu triethylnatriomethantrikarboxylátem v dimethylformamidu a benzenu. Esterové skupiny se poté redukují hydridem lithnohlinitým na triol, čímž se odstraní chránicí skupina. Následuje aktivace konců řetězce přeměnou alkoholových skupin na tosylové pomocí tosylchloridu a pyridinu. Tosyly slouží jako odstupující skupiny v další reakci s trikarboxylátem, při níž vzniká druhá generace. Opakováním předchozích dvou kroků se dají připravit arboroly vyšších generací.[12]
Nejrozšířenějším dendrimerem je poly(amidoamin) (PAMAM). Jeho jádro tvoří diamin (obvykle ethylendiamin), jenž reaguje s methylakrylátem a pak s dalším ethylendiaminem za vzniku PAMAMu generace 0 (G0). Následnými reakcemi se poté získávají produkty vyšších generací, které mají odlišné vlastnosti. Nižší generace nemají žádné znatelné vnitřní oblasti, zatímco (G3 a G4) mají vnitřní prostory zřetelně oddělené od vnější části dendrimeru. Velké (G7 a větší) dendrimery se chovají jako pevné částice s velmi hustými povrchy, což je způsobeno strukturou jejich vnějších vrstev. Funkční skupiny na povrchu dendrimerů lze využít v mnoha oblastech .[14]
Dendrimery mají tři hlavní části: jádro, vnitřní obálku a vnější obálku. Obvykle lze dendrimer připravit tak, aby měl v každé této části jiné funkční skupiny; tím se dají ovlivňovat vlastnosti, jako jsou rozpustnost, tepelná stálost a možnost připojení dalších sloučenin k různým účelům. Velikost a rozvětvenost dendrimeru se také určuje při jeho přípravě. Existují dvě metody syntézy dendrimerů, divergentní a konvergentní. Vzhledem k tomu, že je třeba provést mnoho kroků k ochraně aktivních míst, tak je syntéza některou z těchto metod obtížná. Kvůli tomu jsou dendrimery těžké na přípravu a drahé.
Divergentní metody
editovatDendrimery mají víceúčelová jádra, která jsou rozšiřována posloupnostmi reakcí, jako je Michaelova reakce. Každý krok musí proběhnout úplně, aby se zamezilo chybám ve struktuře dendrimeru, kvůli čemuž by mohly být některé větve kratší než ostatní. Nečistoty mohou způsobit odchylky ve funkcionalitě a symetrii dendrimeru, dosažení čistoty je však obtížné, protože rozdíly mezi správnými a nesprávnými dendrimery bývají malé.[15]
Konvergentní metody
editovatDendrimery lze připravit z malých molekul, které zůstávají navázány na povrch jejich molekul, a reakcemi uvnitř struktury, po kterých se funkční skupiny navazují na jádro. U tohoto postupu je odstraňování nečistot mnohem snadnější a vznikají zde kratší větve, takže vytvořený dendrimer je více monodisperzní. Dendrimery připravené tímto způsobem ovšem nejsou kvůli sterickým efektům tak velké jako ty připravené divergentními metodami.[15]
Click chemie
editovatDendrimery je možné připravit metodami click chemie, jako jsou Dielsovy–Alderovy reakce,[17] thiol-enové a thiol-ynové reakce[18] a reakce azidů s alkyny.[19][20][21]
Vlastnosti
editovatDendrimery a dendrony se vyznačují monodisperzitou a obvykle i vysokou symetričností a sféričností molekul. Dendritické molekuly lze přibližně rozdělit na látky s nízkými a vysokými molárními hmotnostmi. Do první kategorie patří dendrimery a dendrony, do druhé dendronizované polymery, hyperrozvětvené polymery a polymerové kartáče.
Vlastnosti dendrimerů převážně určují funkční skupiny na povrchu molekul, existují však i dendrimery s vnitřními funkcionalitami.[22][23][24]
Dendritické zapouzdření funkčních molekul umožňuje izolaci aktivního místa, struktury napodobující aktivní místa u biomateriálů.[25][26][27]
Lze připravit dendrimery rozpustné ve vodě (což u většiny polymerů není možné), a to funkcionalizací jejich vnějších vrstev nabitými nebo jinými hydrofilními skupinami. K řiditelným vlastnostem patří rovněž toxicita, krystaličnost a chiralita.[3]
Dendrimery mohou být také klasifikovány podle generací, což jsou čísla udávající počet opakujících se rozvětvených cyklů vznikajících v průběhu jejich syntézy. Například dendrimer získaný konvergentní syntézou (na obrázku níže), u něhož byly provedeny rozvětvovací reakce třikrát, se řadí do třetí generace. Každá další přidaná generace přibližně zdvojnásobuje molekulovou hmotnost dendrimeru předchozí generace. Dendrimery vyšších generací mívají více funkčních skupin na povrchu, což je možné využít k úpravě jejich vlastností.[15]
Použití
editovatDendrimery se obvykle používají k připojování dalších sloučenin, které mohou fungovat jako detekční látky, afinitní ligandy, radioligandy, kontrastní látky nebo léčiva. Dendrimery mají pro tato využití velký potenciál, protože jejich struktury mohou tvořit vícevazné systémy; jedna molekula dendrimeru má i stovky míst, kam navázat aktivní látky. Je veden výzkum zaměřený na úpravu hydrofobních prostředí dendritických médií za účelem provádění fotochemických reakcí vytvářejících produkty, jejichž syntéza je jinak obtížná. Byly připraveny ve vodě rozpustné dendrimery zakončené karboxylovými a fenolovými skupinami vhodné pro doručování léčiv i schopné chemických reakcí ve svých vnitřních částech.[28]
Probíhají snahy o navazování zaměřovacích molekul a molekul léčiv na stejný dendrimer, čímž by se omezily vedlejší účinky na zdravé buňky.[14]
Dendrimery také lze použít ke zlepšení rozpustnosti. Od svého zavedení v 80. letech 20. století jsou dendrimery díky své struktuře velkými kandidáty na využití v chemii host–guest.[29]
Dendrimery s hydrofobními jádry a hydrofilními vnějšími částmi mají v roztocích vlastnosti podobné micelám.[30]
Využití dendrimerů jako jednomolekulových micel navrhl George R. Newkome v roce 1985.[31]
Tímto objevem bylo rozvinuto využití dendrimerů ke zlepšování rozpustnosti.[32]
Většina léčiv má hydrofobní vlastnosti, což způsobuje řasu potíží. Tyto nevýhody lze překonat navázáním dendrimerů, které uzavřou do sebe molekuly léčiva a zlepší jejich rozpustnost v důsledku tvorby vodíkových vazeb s vodou.[33][34][35][36][37][38]
Po celém světě probíhá výzkum využití dendrimerů při doručování léčiv[39][40] a cílově specifických nosičů.[41][42][43]
Příkladem dendrimeru s farmaceutickým využitím je polyethoxyethylglycinamidový (PEE-G) dendrimer.[44][45] Tento dendrimer má vysokou HPLC čistotu, je stabilní, rozpustný ve vodě a vykazuje nízkou toxicitu.
Distribuce léčiv
editovatByly vyvinuty postupy pro doručování přírodních látek pomocí polymerních nosičů. Dendrimery se zkoumají pro možné uzavření hydrofobních sloučenin a jejich doručování do buněk. Vlastnosti dendrimerů, jako jsou monodisperzita, rozpustnost ve vodě, schopnost obalení molekul a velké množství navázatelných funkčních skupin a makromolekul z nich činí vhodné kandidáty na doručování léčiv.
Vliv chemických modifikací dendrimeru
editovatDendrimery jsou dobře využitelnými nosiči pro léčiva díky širokému spektru chemických modifikací, které mohou zlepšit jejich využitelnost in vivo a umožňují cílené doručení léčiva na konkrétní místo.
Navázání léčiva na dendrimer lze dosáhnout třemi způsoby (1) kovalentním nebo konjugačním připojením na vnější povrch za vzniku dendrimerového proléčiva, (2) iontovou koordinací na nabité vnější funkční skupiny a (3) micelovitým obalením jeho molekuly.[46][47]
U proléčivové struktury může být vazba léčiva na dendrimer, v závislosti na požadované kinetice, přímá nebo skrz jinou skupinu. Tato skupina by měla být citlivá na pH, odštěpitelná pomocí enzymu, nebo obsahovat disulfidový můstek. Velké množství použitelných skupin zajišťuje rozsáhlé možnosti úpravy vlastností, i připojení další molekuly. Hlavními parametry jsou (1) mechanismus uvolnění po příchodu na cílové místo, ať už v buňce nebo orgánové soustavě, (2) prostorové vlastnosti systému léčivo-dendrimer, které mají zabránit lipofilním molekulám ve skládání do dendrimeru, a (3) rozložitelnost propojující skupiny a následné změny v molekule léčiva.[48][49]
Častou látkou sloužící k pozměnění povrchového náboje a doby cirkulace dendrimerů je polyethylenglykol (PEG). Povrchový náboj má vliv na interakce dendrimerů s biologickými systémy, například dendrimery upravené na aminových koncích interagují s buněčnými membránami skrze aniontové náboje. Některé studie in vivo ukázaly, že polykationtové dendrimery jsou v důsledku zvýšení propustnosti membrán cytotoxické, což lze omezit PEGylacemi aminových skupin, vedoucími k nižší cytotoxicitě a omezení hemolýzy.[50][51]
V dalších studiích bylo zjištěno, že PEGylace dendrimerů zpomaluje uvolňování léčiv, prodlužuje cirkulační časy in vivo a snižuje toxicitu.[52][51]
K úpravě biodistribuce dendrimerů a umožnění jejich zacílení na jednotlivé orgány lze použít mnoho různých funkčních skupin; například folátové receptory mají v nádorových buňkách příliš vysokou míru exprese a jsou tak potenciálními cíli lokalizovaného doručování chemoterapeutik. Konjugací kyseliny listové na PAMAMové dendrimery dochází ke zlepšení cílenosti a k omezení toxických účinků mimo cílové buňky za současného zachování účinků.[52][53]
Zaměřování dendrimerů na cílové buňky pomocí protilátek se také ukázalo jako slibné pro zacílené doručování léčivých látek. Vzhledem k tomu, že jsou EGF receptory v mozkových nádorech často přeexpresované, tak se jedná o vhodné cíle místně specifických léků. Dodávka boru do nádorových buněk je důležitá pro účinnost léčby záchyty neutronů, která vyžaduje vysokou koncentraci boru v nádorových a nízkou koncentraci ve zdravých buňkách. Borovaný dendrimer konjugovaný s monoklonální protilátkou cílící na EGF u krys umožnil k účinné distribuci boru do nádorů.[54][51]
Použití nanočástic dendrimerů s peptidy bylo úspěšné při cílené destrukci HCT-116 buněk karcinomu tlustého střeva. Cílené peptidy lze použít k dosažení místní či buněčné specifity; tyto peptidy vykazují lepší specificitu při spojení s dendrimery. Příkladem může být gemcitabin-YIGSR-CMCht/PAMAM, druh dendrimerové nanočástice, který cíleně ničí tyto nádorové buňky, čehož se dosahuje selektivními interakcemi dendrimeru s lamininovými receptory. Peptidové dendrimery by mohly být využity k přesné distribuci léčiv do nádorových buněk.[55]
Mechanismus příjmu dendrimerů buňkami lze rovněž upravovat pomocí cílených chemických modifikací. Nezměněný PAMAM-G4 dendrimer vstupuje do aktivovaných mikroglií endocytózou v kapalné fázi. Modifikacemi PAMAM-G4 dendrimerů manózou je možné změnit mechanismus internalizace na manózovým receptorem (CD206) řízenou endocytózu. Navázání manózy u králíků mění biodistribuci ve zbytku těla.[56]
Farmakokinetika a farmakodynamika
editovatDendrimery mohou výrazně změnit farmakokinetické a farmakodynamické vlastnosti léčiv. Při použití nosičů není farmakokinetika a farmakodynamika určována vlastnostmi samotného léčiva, ale umístěním dendrimeru, uvolňováním léčivé látky a vylučováním dendrimeru. ADME vlastnosti lze měnit změnami ve velikosti, struktuře a povrchu dendrimeru. Zatímco G9 dendrimery jsou velmi silně distribuovány do jater a sleziny, tak G6 dendrimery mají distribuci výrazně širší. S nárůstem molekulové hmotnosti se zpomaluje vylučování močí a krevní plazmou (prodlužuje se biologický poločas).[50]
Způsoby distribuce
editovatZa účelem zlepšení pohodlí pacienta se často upřednostňuje ústní podání před ostatními způsoby aplikace léku, biodostupnost řady léčiv však v takových případech bývá. Dendrimery mohou zlepšit rozpustnost a stabilitu ústně podaných léčiv a zlepšit jejich průchod přes střevní stěnu.[57] Biodostupnost PAMAMových dendrimerů konjugovaných s léčivými látkami byla zkoumána u myší; zjistilo se, že okolo 9 % dendrimeru se nezměnilo a že ve střevech docházelo k minimálnímu rozkladu dendrimeru.[58]
Nitrožilně podané dendrimery by mohly být využity jako genové vektory k distribuci genů do různých orgánů i nádorů. V jedné studii byly nitrožilně podány PPI dendrimery s genovými komplexy a došlo k expresi těchto genů v játrech, a v jiné podobné injekce pomohly zpomalit růst nádorů u pozorovaných zvířat.[59][60]
Hlavní překážkou při aplikaci přes kůži je pokožka. Hydrofobní léčiva se obtížně dostávají přes kůži, protože se koncentrují v kožním mazu. Použití PAMAMových dendrimerů s nesteroidními antiflogistiky vedlo ke zvýšení hydrofility, které umožnilo lepší průnik léčiva.[61]
Dendrimery mohou být též použity v oftalmologických léčivých přípravcích. T. F. Vanndamme a L. Bobeck použili PAMAMové dendrimery u králíků na dvě modelová léčiva a měřili čas setrvání v očích; ten byl srovnatelný a někdy i větší než u dosud používaných biopolymerů.[62] Tyto výsledky ukázaly, že upravená léčiva mají při použití s dendrimery větší aktivitu a biodostupnost, než bez nich. Konjugáty kyseliny hyaluronové upravitelné pomocí světla, nazývané kyselinové hydrogely, byly použity jako stehy aplikované přímo do oční rohovky. Tyto hydrogelové stehy měly u králíků lepší vlastnosti než tradiční a vedly k nižší tvorbě jizev.[63]
Distribuce léčiv v mozku
editovatPomocí dendrimerů lze efektivně dostat léčiva in vivo skrz hematoencefalickou bariéru. Příkladem je použití PAMAMových dendrimerů s koncovými hydroxyly, které lze zacílit na mozkové makrofágy, což bylo ověřeno fluorescenčně značkovanými dendrimery neutrální generace na králičích modelech mozkové obrny.[64]
Tento postup umožnil provádění distribuce léčiv za mnoha různých podmínek, od mozkové obrny a jiných neurozánětlivých onemocnění po poranění mozku a hypotermickou zástavu oběhu, u řady zvířecích modelů, jako jsou myši, králíci a psi.[65][66][67]
Vstřebávání dendrimeru do mozku přímo souvisí se závažností zánětu a poškozením hematoencefalické bariéry. o kterém se předpokládá, že jde o hlavní faktor umožňující průchod dendrimeru.[68][64]
Dendrimer- s připojeným N-acetylcysteinem vykázal in vivo účinnost jako protizánětlivé léčivo při dávkách přibližně 1000krát nižších než samotné léčivo, což může usnadnit léčbu mozkové obrny, Rettova syndromu, makulární degenerace a jiných zánětlivých nemocí.[64]
Klinické pokusy
editovatExistuje několik produktů obsahujících dendrimery, které jsou schváleny pro použití, nebo u nich probíhají klinické testy. SPL7013, je hyperrozvětvený polymer schválený k léčbě bakteriální vaginózy a k prevenci rozvoje HIV, HPV and HSV v Evropě, jihovýchodní Asii, Japonsku, Kanadě a Austrálii. Vzhledem k účinnosti SPL7013’s vůči širokému spektru virů, byla tato látka testována jako možný lék na SARS-CoV-2. Prvotní in vitro studie ukázaly vysokou účinnost při prevenci nákazy SARS-CoV-2 v buňkách.[69]
Distribuce genů
editovatMožnost dopravit části DNA do požadovaných částí buňky představuje řadu výzev. Výzkum se zaměřuje především na nalezení způsobů dopravy genů do buněk pomocí dendrimerů, aniž by došlo k poškození nebo deaktivaci DNA. K zachování aktivity DNA v průběhu dehydratace se komplexy dendrimerů s DNA obalí polymery rozpustnými ve vodě a následně uzavřou mezi dvě vrstvy funkčního polymeru, který se rychle rozkládá a řídí transfekci genu. Na základě tohoto postupu byly komplexy PAMAMových dendrimerů a DNA použity k obalení biologicky rozložitelných polymerních povlaků pro substrátem řízenou distribuci genů. Rychle se rozkládající funkční polymery mají velký potenciál k využití pro lokalizovanou transfekci.[70][71][72]
Senzory
editovatDendrimery by mohly být použity jako senzory. Zkoumají se systémy, jako jsou snímače pH založené na poly(propylenimin)u,[73] a poly(propylenamin)ové dendrimery první a druhé generace sloužící k fotodetekci kationtů kovů.[74]
Tato oblast je předmětem širokého výzkumu, díky možnosti využití vícenásobné detekce v důsledku většího počtu vazebných míst u dendrimerů.
Nanočástice
editovatDendrimery také mohou sloužit na přípravu monodisperzních kovových nanočástic. Poly(amidoamid)ové (PAMAM) dendrimery mají terciární aminové skupiny v místech, kde se dendrimer rozvětvuje. Kovové ionty se aplikují do vodného roztoku dendrimeru a vytvoří komplex s volnými elektronovými páry na terciárních aminech. Následně jsou ionty redukovány na oxidační číslo 0, čímž se utvoří nanočástice uzavřené v dendrimeru. Tyto nanočástice mívají velikosti mezi 1,5 a 10 nanometry.[75]
Ostatní použití
editovatVzhledem k častému používání herbicidů a insekticidů v zemědělství nacházejí dendrimery využití i při zlepšování distribuce agrochemikálií za účelem zlepšení růstu plodin a boji proti rostlinným chorobám.[76]
Dendrimery jsou také zkoumány jako náhrady krve. Jejich velké molekuly obklopující centrum napodobující hem výrazně omezuje míru degradace[77][78] a cytotoxicity oproti volnému hemu.
Dendritický funkční polymer polyamidoamin (PAMAM) se používá na přípravu mikrokapslí a na výrobu samoopravujících nátěrů.[79][80]
Odkazy
editovatSouvisející články
editovatExterní odkazy
editovat- Obrázky, zvuky či videa k tématu Dendrimer na Wikimedia Commons
Reference
editovatV tomto článku byl použit překlad textu z článku Dendrimer na anglické Wikipedii.
- ↑ D. Astruc; E. Boisselier; C. Ornelas. Dendrimers designed for functions: from physical, photophysical, and supramolecular properties to applications in sensing, catalysis, molecular electronics, photonics, and nanomedicine. Chemical Reviews. 2010, s. 1857–1959. DOI 10.1021/cr900327d. PMID 20356105.
- ↑ Vögtle, Fritz / Richardt, Gabriele / Werner, Nicole Dendrimer Chemistry Concepts, Syntheses, Properties, Applications 2009 ISBN 3-527-32066-0
- ↑ a b B. K. Nanjwade; H. M. Bechra; G. K. Derkar; F. V. Manvi; V. K. Nanjwade. Dendrimers: emerging polymers for drug-delivery systems. European Journal of Pharmaceutical Sciences. 2009, s. 185–196. DOI 10.1016/j.ejps.2009.07.008. PMID 19646528.
- ↑ Single-Crystal Structures of Polyphenylene Dendrimers. Chemistry: A European Journal. 2002, s. 3858–3864. DOI 10.1002/1521-3765(20020902)8:17<3858::AID-CHEM3858>3.0.CO;2-5.
- ↑ B. E. Hirsch; S. Lee; B. Qiao; C. H. Chen; K. P. McDonald; S. L. Tait; A. H. Flood. Anion-induced dimerization of 5-fold symmetric cyanostars in 3D crystalline solids and 2D self-assembled crystals. Chemical Communications. 2014, s. 9827–9830. Dostupné online. DOI 10.1039/C4CC03725A. PMID 25080328.
- ↑ E. Buhleier; W. Wehner; F. Vögtle. "Cascade"- and "Nonskid-Chain-like" Syntheses of Molecular Cavity Topologies. Synthesis. 1978, s. 155–158. DOI 10.1055/s-1978-24702.
- ↑ Šablona:US Patent Denkewalter, Robert G., Kolc, Jaroslav, Lukasavage, William J.
- ↑ Denkewalter, Robert G. et al. (1981) "Macromolecular highly branched homogeneous compound" Šablona:US Patent
- ↑ Tomalia, Donald A. and Dewald, James R. (1983) "Dense star polymers having core, core branches, terminal groups" Šablona:US Patent
- ↑ A New Class of Polymers: Starburst-Dendritic Macromolecules. Polymer Journal. 1985, s. 117–132. DOI 10.1295/polymj.17.117.
- ↑ Treelike molecules branch out – chemist Donald A. Tomalia synthesized first dendrimer molecule – Chemistry – Brief Article. Science News. 1996. Dostupné online.
- ↑ a b G. R. Newkome; Z. Yao; G. R. Baker; V. K. Gupta. Micelles. Part 1. Cascade molecules: a new approach to micelles. A [27]-arborol. The Journal of Organic Chemistry. 1985, s. 2003–2004. DOI 10.1295/polymj.17.117.
- ↑ C. J. Hawker; J. M. Fréchet. Preparation of polymers with controlled molecular architecture. A new convergent approach to dendritic macromolecules. Journal of the American Chemical Society. 1990, s. 7638–7647. DOI 10.1021/ja00177a027.
- ↑ a b Greg T. Hermanson. Bioconjugate Techniques. London: Academic Press of Elsevier, 2008. Dostupné online. ISBN 978-0-12-370501-3. Kapitola 7.
- ↑ a b c P. Holister; T. Harper. Dendrimers: Technology White Papers [online]. Cientifica, 2003 [cit. 2010-03-17]. Dostupné v archivu pořízeném z originálu dne 2011-07-06.
- ↑ Frank Morgenroth; Erik Reuther; Klaus Müllen. Polyphenylene Dendrimers: From Three-Dimensional to Two-Dimensional Structures. Angewandte Chemie International Edition in English. 1997, s. 631–634. DOI 10.1002/anie.199706311.
- ↑ G. Franc; A. K. Kakkar. Diels-Alder "click" chemistry in designing dendritic macromolecules. Chemistry. 2009, s. 5630–5639. DOI 10.1002/chem.200900252. PMID 19418515.
- ↑ K. L. Killops; L. M. Campos; C. J. Hawker. Robust, efficient, and orthogonal synthesis of dendrimers via thiol-ene "click" chemistry. Journal of the American Chemical Society. 2008, s. 5062–5064. DOI 10.1021/ja8006325. PMID 18355008.
- ↑ K. Noda; Y. Minatogawa; T. Higuchi. Effects of hippocampal neurotoxicant, trimethyltin, on corticosterone response to a swim stress and glucocorticoid binding capacity in the hippocampus in rats. The Japanese Journal of Psychiatry and Neurology. 1991, s. 107–108. PMID 1753450.
- ↑ J. P. Machaiah. Changes in macrophage membrane proteins in relation to protein deficiency in rats. Indian Journal of Experimental Biology. 1991, s. 463–467. PMID 1916945.
- ↑ G. Franc; A. Kakkar. Dendrimer design using Cu(I)-catalyzed alkyne-azide "click-chemistry". Chemical Communications. 2008, s. 5267–5276. DOI 10.1039/b809870k. PMID 18985184.
- ↑ P. Antoni; Y. Hed; A. Nordberg; D. Nyström; H. von Holst; A. Hult; M. Malkoch. Bifunctional dendrimers: from robust synthesis and accelerated one-pot postfunctionalization strategy to potential applications. Angewandte Chemie. 2009, s. 2126–2130. DOI 10.1002/anie.200804987.
- ↑ J. R. McElhanon; D. V. McGrath. Toward chiral polyhydroxylated dendrimers. Preparation and chiroptical properties. The Journal of Organic Chemistry. 2000, s. 3525–3529. DOI 10.1021/jo000207a. PMID 10843641.
- ↑ C. O. Liang; J. M. Fréchet. Incorporation of Functional Guest Molecules into an Internally Functionalizable Dendrimer through Olefin Metathesis. Macromolecules. 2005, s. 6276–6284. DOI 10.1021/ma050818a. Bibcode 2005MaMol..38.6276L.
- ↑ S. Hecht; J. M. Fréchet. Dendritic Encapsulation of Function: Applying Nature's Site Isolation Principle from Biomimetics to Materials Science. Angewandte Chemie. 2001, s. 74–91. DOI 10.1002/1521-3773(20010105)40:1<74::AID-ANIE74>3.0.CO;2-C. PMID 11169692.
- ↑ M. Fischer; F. Vögtle. Dendrimers: From Design to Application—A Progress Report. Angewandte Chemie International Edition. 1999, s. 884–905. DOI 10.1002/(SICI)1521-3773(19990401)38:7<884::AID-ANIE884>3.0.CO;2-K.
- ↑ Frechet J, Tomalia DA. Dendrimers and Other Dendritic Polymers. New York, NY: John Wiley & Sons, March 2002. ISBN 978-0-471-63850-6.
- ↑ L. S. Kaanumalle; R. Ramesh; V. S. Murthy Maddipatla; J. Nithyanandhan; N. Jayaraman; V. Ramamurthy. Dendrimers as photochemical reaction media. Photochemical behavior of unimolecular and bimolecular reactions in water-soluble dendrimers. The Journal of Organic Chemistry. 2005, s. 5062–5069. DOI 10.1021/jo0503254. PMID 15960506.
- ↑ Donald A. Tomalia; Adel M. Naylor; William A. Goddard. Starburst Dendrimers: Molecular-Level Control of Size, Shape, Surface Chemistry, Topology, and Flexibility from Atoms to Macroscopic Matter. Angewandte Chemie International Edition in English. 1990, s. 138–175. DOI 10.1002/anie.199001381.
- ↑ J. M. Fréchet. Functional polymers and dendrimers: reactivity, molecular architecture, and interfacial energy. Science. 1994, s. 1710–1715. DOI 10.1126/science.8134834. PMID 8134834. Bibcode 1994Sci...263.1710F.
- ↑ M. Liu; K. Kono; J. M. Fréchet. Water-soluble dendritic unimolecular micelles: their potential as drug delivery agents. Journal of Controlled Release. 2000, s. 121–131. DOI 10.1016/s0168-3659(99)00245-x. PMID 10699276.
- ↑ George R. Newkome; Zhongqi Yao; Gregory R. Baker; Vinod K. Gupta. Micelles Part 1. Cascade molecules: a new approach to micelles, A-arborol. The Journal of Organic Chemistry. 1985, s. 155–158. DOI 10.1021/jo00211a052.
- ↑ S. Stevelmens; J. C. Hest; J. F. Jansen; D. A. Boxtel; E. W. Miejer. Synthesis, characterisation and guest-host properties of inverted unimolecular micelles. Journal of the American Chemical Society. 1996, s. 7398–7399. Dostupné online. DOI 10.1021/ja954207h.
- ↑ U. Gupta; H. B. Agashe; A. Asthana; N. K. Jain. Dendrimers: novel polymeric nanoarchitectures for solubility enhancement. Biomacromolecules. 2006, s. 649–658. DOI 10.1021/bm050802s. PMID 16529394.
- ↑ T. P. Thomas; I. J. Majoros; A. Kotlyar; J. F. Kukowska-Latallo; A. Bielinska; A. Myc; J. R. Baker. Targeting and inhibition of cell growth by an engineered dendritic nanodevice. Journal of Medicinal Chemistry. 2005, s. 3729–3735. DOI 10.1021/jm040187v. PMID 15916424.
- ↑ D. Bhadra; S. Bhadra; P. Jain; N. K. Jain. Pegnology: a review of PEG-ylated systems. Die Pharmazie. 2002, s. 5–29. PMID 11836932.
- ↑ A. Asthana; A. S. Chauhan; P. V. Diwan; N. K. Jain. Poly(amidoamine) (PAMAM) dendritic nanostructures for controlled site-specific delivery of acidic anti-inflammatory active ingredient. AAPS PharmSciTech. 2005, s. E536-542. DOI 10.1208/pt060367. PMID 16354015.
- ↑ D. Bhadra; S. Bhadra; S. Jain; N. K. Jain. A PEGylated dendritic nanoparticulate carrier of fluorouracil. International Journal of Pharmaceutics. 2003, s. 111–124. DOI 10.1016/s0378-5173(03)00132-7. PMID 12711167.
- ↑ A. J. Khopade; F. Caruso; P. Tripathi; S. Nagaich; N. K. Jain. Effect of dendrimer on entrapment and release of bioactive from liposomes. International Journal of Pharmaceutics. 2002, s. 157–162. DOI 10.1016/S0378-5173(01)00901-2.
- ↑ R. N. Prajapati; R. K. Tekade; U. Gupta; V. Gajbhiye; N. K. Jain. Dendimer-mediated solubilization, formulation development and in vitro-in vivo assessment of piroxicam. Molecular Pharmaceutics. 2009, s. 940–950. DOI 10.1021/mp8002489. PMID 19231841.
- ↑ Dendrimer-mediated transdermal delivery: enhanced bioavailability of indomethacin. Journal of Controlled Release. 2003, s. 335–343. DOI 10.1016/s0168-3659(03)00200-1. PMID 12880700.
- ↑ Nanoparticle targeting of anticancer drug improves therapeutic response in animal model of human epithelial cancer. Cancer Research. 2005, s. 5317–5324. DOI 10.1016/s0168-3659(03)00200-1. PMID 12880700.
- ↑ Design and function of a dendrimer-based therapeutic nanodevice targeted to tumor cells through the folate receptor. Pharmaceutical Research. 2002, s. 1310–1316. Dostupné online. DOI 10.1023/a:1020398624602. PMID 12403067.
- ↑ Poly Ethoxy Ethyl Glycinamide (PEE-G) Dendrimers: Dendrimers Specifically Designed for Pharmaceutical Applications. ChemMedChem. 2016, s. 1583–1586. DOI 10.1002/cmdc.201600270. PMID 27390296.
- ↑ GLYCOSYN. PEE-G Dendrimers [online]. Dostupné online.
- ↑ Dendrimer-encapsulated camptothecins: increased solubility, cellular uptake, and cellular retention affords enhanced anticancer activity in vitro. Cancer Research. 2006, s. 11 913 – 11 921. DOI 10.1158/0008-5472.CAN-06-2066. PMID 17178889.
- ↑ R. K. Tekade; T. Dutta; V. Gajbhiye; N. K. Jain. Exploring dendrimer towards dual drug delivery: pH responsive simultaneous drug-release kinetics. Journal of Microencapsulation. 2009, s. 287–296. DOI 10.1080/02652040802312572. PMID 18791906.
- ↑ Doxorubicin Conjugation and Drug Linker Chemistry Alter the Intravenous and Pulmonary Pharmacokinetics of a PEGylated Generation 4 Polylysine Dendrimer in Rats. Journal of Pharmaceutical Sciences. 2018, s. 2509–2513. Dostupné online. DOI 10.1016/j.xphs.2018.05.013. PMID 29852134.
- ↑ S. da Silva Santos; E. Igne Ferreira; J. Giarolla. Dendrimer Prodrugs. Molecules. 2016, s. 686. DOI 10.3390/molecules21060686. PMID 27258239.
- ↑ a b L. M. Kaminskas; B. J. Boyd; C. J. Porter. Dendrimer pharmacokinetics: the effect of size, structure and surface characteristics on ADME properties. Nanomedicine. 2011, s. 1063–1084. DOI 10.2217/nnm.11.67. PMID 21955077.
- ↑ a b c D. Luong; P. Kesharwani; R. Deshmukh; M. C. Mohd Amin; U. Gupta; K. Greish; A. K. Iyer. PEGylated PAMAM dendrimers: Enhancing efficacy and mitigating toxicity for effective anticancer drug and gene delivery. Acta Biomaterialia. 2016, s. 14–29. DOI 10.1016/j.actbio.2016.07.015. PMID 27422195.
- ↑ a b P. Singh; U. Gupta; A. Asthana; N. K. Jain. Folate and folate-PEG-PAMAM dendrimers: synthesis, characterization, and targeted anticancer drug delivery potential in tumor bearing mice. Bioconjugate Chemistry. 2008, s. 2239–2252. DOI 10.1021/bc800125u. PMID 18950215.
- ↑ I. J. Majoros; C. R. Williams; A. Becker; J. R. Baker. Methotrexate delivery via folate targeted dendrimer-based nanotherapeutic platform. Wiley Interdisciplinary Reviews. Nanomedicine and Nanobiotechnology. 2009, s. 502–510. DOI 10.1002/wnan.37. PMID 20049813.
- ↑ G. Wu; R. F. Barth; W. Yang; M. Chatterjee; W. Tjarks; M. J. Ciesielski; R. A. Fenstermaker. Site-specific conjugation of boron-containing dendrimers to anti-EGF receptor monoclonal antibody cetuximab (IMC-C225) and its evaluation as a potential delivery agent for neutron capture therapy. Bioconjugate Chemistry. 2004, s. 185–194. DOI 10.1021/bc0341674. PMID 14733599.
- ↑ Carvalho MR, Carvalho CR, Maia FR, Caballero D, Kundu SC, Reis RL, Oliveira JM. Peptide‐Modified Dendrimer Nanoparticles for Targeted Therapy of Colorectal Cancer. Advanced Therapeutics. November 2019, s. 1900132. ISSN 2366-3987. DOI 10.1002/adtp.201900132. S2CID 203135854.
- ↑ A. Sharma; J. E. Porterfield; E. Smith; R. Sharma; S. Kannan; R. M. Kannan. Effect of mannose targeting of hydroxyl PAMAM dendrimers on cellular and organ biodistribution in a neonatal brain injury model. Journal of Controlled Release. 2018, s. 175–189. DOI 10.1016/j.jconrel.2018.06.003. PMID 29883694.
- ↑ N. Csaba; M. Garcia-Fuentes; M. J. Alonso. The performance of nanocarriers for transmucosal drug delivery. Expert Opinion on Drug Delivery. 2006, s. 463–478. DOI 10.1517/17425247.3.4.463. PMID 16822222.
- ↑ G. Thiagarajan; S. Sadekar; K. Greish; A. Ray; H. Ghandehari. Evidence of oral translocation of anionic G6.5 dendrimers in mice. Molecular Pharmaceutics. 2013, s. 988–998. DOI 10.1021/mp300436c. PMID 23286733.
- ↑ C. Dufès; I. F. Uchegbu; A. G. Schätzlein. Dendrimers in gene delivery. Advanced Drug Delivery Reviews. 2005, s. 2177–2202. Dostupné online. DOI 10.1016/j.addr.2005.09.017. PMID 16310284.
- ↑ C. Dufès; W. N. Keith; A. Bilsland; I. Proutski; I. F. Uchegbu; A. G. Schätzlein. Synthetic anticancer gene medicine exploits intrinsic antitumor activity of cationic vector to cure established tumors. Cancer Research. 2005, s. 8079–8084. DOI 10.1158/0008-5472.CAN-04-4402. PMID 16166279.
- ↑ Y. Cheng; N. Man; T. Xu; R. Fu; X. Wang; X. Wang; L. Wen. Transdermal delivery of nonsteroidal anti-inflammatory drugs mediated by polyamidoamine (PAMAM) dendrimers. Journal of Pharmaceutical Sciences. 2007, s. 595–602. DOI 10.1002/jps.20745. PMID 17094130.
- ↑ T. F. Vandamme; L. Brobeck. Poly(amidoamine) dendrimers as ophthalmic vehicles for ocular delivery of pilocarpine nitrate and tropicamide. Journal of Controlled Release. 2005, s. 23–38. DOI 10.1016/j.jconrel.2004.09.015. PMID 15653131.
- ↑ Q. Xu; S. P. Kambhampati; R. M. Kannan. Nanotechnology approaches for ocular drug delivery. Middle East African Journal of Ophthalmology. 2013, s. 26–37. Dostupné online. DOI 10.4103/0974-9233.106384. PMID 23580849.
- ↑ a b c Intrinsic targeting of inflammatory cells in the brain by polyamidoamine dendrimers upon subarachnoid administration. Nanomedicine. 2010, s. 1317–1329. DOI 10.2217/nnm.10.89. PMID 21128716.
- ↑ Dendrimer-based postnatal therapy for neuroinflammation and cerebral palsy in a rabbit model. Science Translational Medicine. 2012, s. 130–146. DOI 10.1126/scitranslmed.3003162. PMID 22517883.
- ↑ Dendrimer brain uptake and targeted therapy for brain injury in a large animal model of hypothermic circulatory arrest. ACS Nano. 2014, s. 2134–2147. DOI 10.1021/nn404872e. PMID 24499315.
- ↑ G. Kannan € autor2 = S. P. Kambhampati; S. R. Kudchadkar. Effect of anesthetics on microglial activation and nanoparticle uptake: Implications for drug delivery in traumatic brain injury. Journal of Controlled Release. 2017, s. 192–199. DOI 10.1016/j.jconrel.2017.03.032. PMID 28336376.
- ↑ Dendrimer-mediated delivery of N-acetyl cysteine to microglia in a mouse model of Rett syndrome. Journal of Neuroinflammation. 2017, s. 252. DOI 10.1186/s12974-017-1004-5. PMID 29258545.
- ↑ Starpharma (ASX:SPL) compound shows activity against coronavirus - The Market Herald [online]. The Market Herald, 2020-04-16 [cit. 2020-04-30]. Dostupné online.[nedostupný zdroj]
- ↑ H. L. Fu; S. X. Cheng; X. Z. Zhang; R. X. Zhuo. Dendrimer/DNA complexes encapsulated functional biodegradable polymer for substrate-mediated gene delivery. The Journal of Gene Medicine. 2008, s. 1334–1342. DOI 10.1002/jgm.1258. PMID 18816481.
- ↑ H. L. Fu; S. X. Cheng; X. Z. Zhang; R. X. Zhuo. Dendrimer/DNA complexes encapsulated in a water soluble polymer and supported on fast degrading star poly(DL-lactide) for localized gene delivery. Journal of Controlled Release. 2007, s. 181–188. DOI 10.1016/j.jconrel.2007.08.031. PMID 17900738.
- ↑ T. Dutta; M. Garg; N. K. Jain. Poly(propyleneimine) dendrimer and dendrosome mediated genetic immunization against hepatitis B. Journal of Controlled Release. 2008, s. 3389–3394. DOI 10.1016/j.vaccine.2008.04.058. PMID 10.1016/j.vaccine.2008.04.05.
- ↑ E. G. Fernandes; N. C.; A. A. de Queiroz; F. E. Guimaraes; V. Zucolotto. Immobilization of Poly(propylene imine) Dendrimer/Nickel Phthalocyanine as Nanostructured Multilayer Films To Be Used as Gate Membranes for SEGFET pH Sensors. Journal of Physical Chemistry C. 2010, s. 6478–6483. DOI 10.1021/jp9106052.
- ↑ I. Grabchev; D. Staneva; J. M. Chovelon. Photophysical investigations on the sensor potential of novel, poly(propylenamine) dendrimers modified with 1,8-naphthalimide units. Dyes and Pigments. 2010, s. 189–193. DOI 10.1016/j.dyepig.2009.10.023.
- ↑ R. W. Scott; O. M. Wilson; R. M. Crooks. Synthesis, characterization, and applications of dendrimer-encapsulated nanoparticles. The Journal of Physical Chemistry B. 2005, s. 692–704. DOI 10.1021/jp0469665. PMID 16866429.
- ↑ Dendrimer technology licensed for herbicide [online]. www.labonline.com.au [cit. 2016-09-25]. Dostupné online.
- ↑ L. J. Twyman; Y. Ge. Porphyrin cored hyperbranched polymers as heme protein models. Chemical Communications. 2006, s. 1658–1660. DOI 10.1039/b600831n. PMID 16583011.
- ↑ L. J. Twyman; A. Ellis; P. J. Gittins. Pyridine encapsulated hyperbranched polymers as mimetic models of haeme containing proteins, that also provide interesting and unusual porphyrin-ligand geometries. Chemical Communications. 2012, s. 154–156. DOI 10.1039/c1cc14396d. PMID 22039580.
- ↑ Tatiya, Pyus D., et al. "Novel polyurea microcapsules using dendritic functional monomer: synthesis, characterization, and its use in self-healing and anticorrosive polyurethane coatings." Industrial & Engineering Chemistry Research 52.4 (2013): 1562-1570
- ↑ Chaudhari, Ashok B., et al. "Polyurethane prepared from neem oil polyesteramides for self-healing anticorrosive coatings." Industrial & Engineering Chemistry Research 52.30 (2013): 10189-10197