Trans-1,2-diaminocyklohexan
trans-1,2-Diaminocyklohexan je organická sloučenina se vzorcem C6H10(NH2)2. Používá se na přípravu chirálních ligandů používaných jako katalyzátory v asymetrické syntéze.[2] Získává se hydrogenací o-fenylendiaminu, při které vzniká společně s cis-izomerem. Rovněž může vzniknout jako vedlejší produkt při hydrogenaci adiponitrilu. Racemický trans-izomer lze rozdělit na enantiomery (směs (1R,2R)-1,2-diaminocyklohexanu a (1S,2S)-1,2-diaminocyklohexanu v poměru 1:1) pomocí enantiomerně čisté kyseliny vinné.[3]
| trans-1,2-Diaminocyklohexan | |
|---|---|
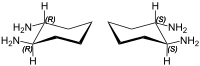 Strukturní vzorce obou enantiomerů trans-1,2-diaminocyklohexanu | |
| Obecné | |
| Systematický název | (±)-trans-cyklohexan-1,2-diamin |
| Ostatní názvy | 1,2-diaminocyklohexan |
| Sumární vzorec | C6H14N2 |
| Vzhled | bezbarvá kapalina |
| Identifikace | |
| Registrační číslo CAS | 21436-03-3 |
| PubChem | 479307 |
| SMILES | N[C@H]1CCCC[C@@H]1N |
| InChI | InChI=1S/C6H14N2/c7-5-3-1-2-4-6(5)8/h5-6H,1-4,7-8H2/t5-,6-/m0/s1 |
| Vlastnosti | |
| Molární hmotnost | 114,19 g/mol |
| Teplota tání | 14 až 15 °C (287 až 288 K) |
| Teplota varu | 79 až 81 °C (352 až 354 K) |
| Hustota | 0,951 g/cm3 |
| Bezpečnost | |
| [1] Nebezpečí[1] | |
Některá data mohou pocházet z datové položky. | |
Odvozené ligandy
editovatZ (1R,2R)- nebo (1S,2S)-1,2-diaminocyklohexanu lze připravit další ligandy, jako jsou analogy salenu, používané při Jacobsenově epoxidaci, a kyselina diaminocyklohexantetraoctová.
Reference
editovatV tomto článku byl použit překlad textu z článku Trans-1,2-Diaminocyclohexane na anglické Wikipedii.
- ↑ a b (1R,2R)-(-)-1,2-Diaminocyclohexane. pubchem.ncbi.nlm.nih.gov [online]. PubChem [cit. 2021-05-24]. Dostupné online. (anglicky)
- ↑ Cyrille Kouklovsky, Yves Langlois "(1S,2S)-1,2-Diaminocyclohexane" in Encyclopedia of Reagents for Organic Synthesis, 2003; John Wiley & Sons. DOI:10.1002/047084289X.rn00145
- ↑ JAY F. LARROW AND ERIC N. JACOBSEN. (R,R)-N,N'-Bis(3,5-Di-tert-Butylsalicylidene)-1,2-Cyclohexanediamino Manganese(III) Chloride, A Highly Enantioselective Epoxidation Catalyst. Org. Synth.. 2004. Dostupné online.; Coll. Vol.. S. 96.

