Benzyl-chlorformiát
Benzyl-chlorformiát je organická sloučenina, ester kyseliny chlormravenčí a benzylalkoholu. Dá se na něj nahlížet i jako na chlorid benzyloxykarbonylové. V čisté podobě se jedná o bezbarvou (i když běžně dodávané vzorky mohou být nažloutlé) olejovitou kapalinu citlivou na přítomnost vody.
| Benzylchlorformiát | |
|---|---|
 Strukturní vzorec | |
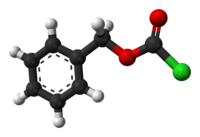 Model molekuly | |
| Obecné | |
| Systematický název | benzylkarbonochloridát |
| Ostatní názvy | benzylchlorformiát |
| Sumární vzorec | C8H7ClO2 |
| Vzhled | bezbarvá kapalina[1] |
| Identifikace | |
| Registrační číslo CAS | 501-53-1 |
| EC-no (EINECS/ELINCS/NLP) | 207-925-0 |
| PubChem | 10387 |
| SMILES | C1=CC=C(C=C1)COC(=O)Cl |
| InChI | InChI=1S/C8H7ClO2/c9-8(10)11-6-7-4-2-1-3-5-7/h1-5H,6H2 |
| Vlastnosti | |
| Molární hmotnost | 170,59 g/mol |
| Teplota tání | 0 °C (273 K)[1] |
| Teplota varu | 152 °C (425 K)[1] |
| Hustota | 1,2166 g/cm3 (20 °C)[1] |
| Rozpustnost ve vodě | reaguje[1] |
| Rozpustnost v polárních rozpouštědlech | rozpustný v acetonu[1] |
| Rozpustnost v nepolárních rozpouštědlech | rozpustný v benzenu a diethyletheru[1] |
| Tlak páry | 9 Pa (85-87 °C)[1] |
| Bezpečnost | |
| [1] | |
| H-věty | H314 H400 H410[1] |
| P-věty | P260 P264 P273 P280 P301+330+331 P302+361+354 P304+340 P305+354+338 P316 P363 P391 P405 P501[1] |
| Teplota vzplanutí | 80 °C (353 K)[1] |
Některá data mohou pocházet z datové položky. | |
Tuto sloučeninu poprvé připravil Leonidas Zervas ve 30. letech 20. století za účelem zavádění benzyloxykarbonylových chránicích skupin do molekul, které se stalo základem Bergmannovy-Zervasovy karboxybenzylové syntézy peptidů, již společně s ním vyvinul Max Bergmann.[2][3]
Jednalo se o první provedenou řízenou umělou syntézu peptidů; do 50. let šlo o nejčastěji používaný postup.[2] Benzylchlorformiát se stále používá na ochranu aminových skupin.
Příprava
editovatTato sloučenina se připravuje reakcí benzylalkoholu s fosgenem:
- PhCH2OH + COCl2 → PhCH2OC(O)Cl + HCl
Fosgen se používá v přebytku, aby se omezila tvorba karbonátu (PhCH2O)2C=O.[4]
Používání fosgenu je nebezpečné, první výzkumníci v této oblasti trpěli kvůli němu chronickými plicními nemocemi.[5]
Chránicí skupiny u aminů
editovatBenzylchlorformiát se používá v organické syntéze na připojování benzyloxykarbonylových (Cbz nebo Z), benzylchlorformiát tak lze zkráceně zapsat jako Cbz-Cl či Z-Cl.
Benzyloxykarbonylové skupiny omezují nukleofilitu a zásaditost volných elektronových párů na atomech dusíku. Tímto se brání racemizaci aminů a vzniklé chráněné aminy jsou základem Bergmannovy-Zervasovy syntézy oligopeptidů.
Obecný průběh reakce sloužící k ochraně N-konce narůstajícího řetězce peptidu vypadá takto:[2][3]
Tato reakce je považována za přelomovou a považuje se za zvrat v oblasti chemie syntetických peptidů.[2] Překonána byla až na začátku 50. let 20. století postupy založenými na smíšených anhydridech a aktivovaných esterech.
Přestože se tato reakce již u peptidů nepoužívá, tak je stále velmi rozšířená při chránění aminů v organické syntéze, například při totálních syntézách. Navazování chránicích skupin s využitím benzylchlorformiátu se obvykle provádí jedním z těchto způsobů:
- Benzylchlorformiát a zásada, například uhličitan sodný, ve vodě za teploty 0 °C[3]
- Benzylchlorformiát a oxid hořečnatý v ethylacetátu za 70 °C[6]
- Benzylchlorformiát, N,N-diisopropylethylamin (DIPEA), acetonitril a trifluormethansulfonát skanditý (Sc(OTf)3)[7]
Cbz skupiny lze vytvořit také reakcemi izokyanátů s benzylalkoholem (podobně jako v Curtiově přesmyku).
Odstranění chránicí skupiny
editovatK odstraňování Cbz skupin se většinou používají hydrogenolýzy za přítomnosti palladiových katalyzátorů,[2][8] jako je palladium na uhlíku.[9]
Další množnost představuje použití kyseliny bromovodíkové se silnými Lewisovými kyselinami, za současného zachytávání vznikajících benzylových karbokationtů.[10]
Také lze použít 2-merkaptoethanol s fosforečnanem draselným v dimethylacetamidu.[11]
Při ochraňování aminů některým z výše uvedených postupů vznikají koncové karbamové kyseliny, které se poté rychle dekarboxylují za uvolnění aminů.
Odkazy
editovatExterní odkazy
editovat- Obrázky, zvuky či videa k tématu Benzyl-chlorformiát na Wikimedia Commons
Reference
editovatV tomto článku byl použit překlad textu z článku Benzyl chloroformate na anglické Wikipedii.
- ↑ a b c d e f g h i j k l https://pubchem.ncbi.nlm.nih.gov/compound/10387
- ↑ a b c d e P. G. Katsoyannis. The Chemistry of Polypeptides. New York: Plenum Press, 1973. Dostupné online. ISBN 978-1-4613-4571-8. DOI 10.1007/978-1-4613-4571-8. Archivováno 13. 10. 2022 na Wayback Machine.
- ↑ a b c Max Bergmann; Leonidas Zervas. Über ein allgemeines Verfahren der Peptid-Synthese. Berichte der deutschen chemischen Gesellschaft. 1932, s. 1192–1201. DOI 10.1002/cber.19320650722.
- ↑ L. Hough; J. E. Priddle. Carbonate derivatives of methyl α-D-mannopyranoside and of D-mannose. Journal of the Chemical Society. 1961, s. 3178–3181. DOI 10.1039/JR9610003178.
- ↑ I. Theodorakopoulos; G. Tsatsas. Dedication to Prof. L. Zervas (from the Minutes of the Academy of Athens). org.chem.uoa.gr. 1981, s. 3178–3181. Dostupné online [cit. 2021-03-31]. DOI 10.1039/JR9610003178. Archivováno 19. 12. 2021 na Wayback Machine.
- ↑ M. Dymicky. Preparation of Carbobenzoxy-L-Tyrosine Methyl and Ethyl Esters and of the Corresponding Carbobenzoxy Hydrazides. Organic Preparations and Procedures International. 1989, s. 83–90. ISSN 0030-4948. DOI 10.1080/00304948909356350.
- ↑ Varinder K. Aggarwal; Paul S. Humphries; Ashley Fenwick. A Formal Asymmetric Synthesis of Anatoxin-a Using an Enantioselective Deprotonation Strategy on an Eight-Membered Ring. Angewandte Chemie International Edition. 1999, s. 1985–1986. ISSN 0030-4948. DOI 10.1002/(SICI)1521-3773(19990712)38:13/14<1985::AID-ANIE1985>3.0.CO;2-7. PMID 34182674.
- ↑ Hans-Dieter Jakubke; Norbert Sewald. Peptides from A to Z: A Concise Encyclopedia. [s.l.]: John Wiley & Sons, 2008. ISBN 978-3-527-62117-0. DOI 10.1002/(SICI)1521-3773(19990712)38:13/14<1985::AID-ANIE1985>3.0.CO;2-7. PMID 34182674.
- ↑ François-Xavier Felpin; Eric Fouquet. A Useful, Reliable and Safer Protocol for Hydrogenation and the Hydrogenolysis of O-Benzyl Groups: The In Situ Preparation of an Active Pd0/C Catalyst with Well-Defined Properties. Chemistry – A European Journal. 2010-11-02. ISSN 1521-3765. DOI 10.1002/chem.201001377. PMID 20845414.
- ↑ Theodora W. Greene; Peter G. M. Wuts. Protecting Groups in Organic Synthesis. [s.l.]: J. Wiley, 1999. DOI isbn = 978-0-471-16019-9.
- ↑ Thomas Scattolin; Tawfik Gharbaoui; Cheng-yi Chen. Nucleophilic Deprotection of Carbamate Mediated by 2-Mercaptoethanol. Organic Letters. 2022. DOI 10.1021/acs.orglett.2c01410. PMID 35559611.

